
Contoh Soal Hidrolisis Asam Lemah Dan Basa Lemah
Pengertian Hidrolisis. Hidrolisis berasal dari bahasa Yunani Kuno yaitu Hidro yang berarti "Air" dan Lisis yang berarti "tidak mengikat". Setiap reaksi kimia pada hidrolisis dimana molekul air memecah satu atau lebih ikatan kimia. Istilah hidrolisis secara luas digunakan untuk reaksi substitusi, eliminasi dan solvaso dimana air adalah.

Rumus Hidrolisis Total Pemburu Soal Jawaban Riset
Hidrolisis adalah ciri reaksi kimia yang dekomposisi di mana salah satu reaktan adalah air dan biasanya air tersebutlah yang dipergunakan untuk memutus ikatan kimia dalam reaktan lainnya. Persamaan umum dari reaksi hidrolisis adalah: AB + H 2 O → AH + BOH Reaksi hidrolisis organik melibatkan reaksi air dan ester: RCO-OR '+ H 2 O → RCO-OH + R'-OH
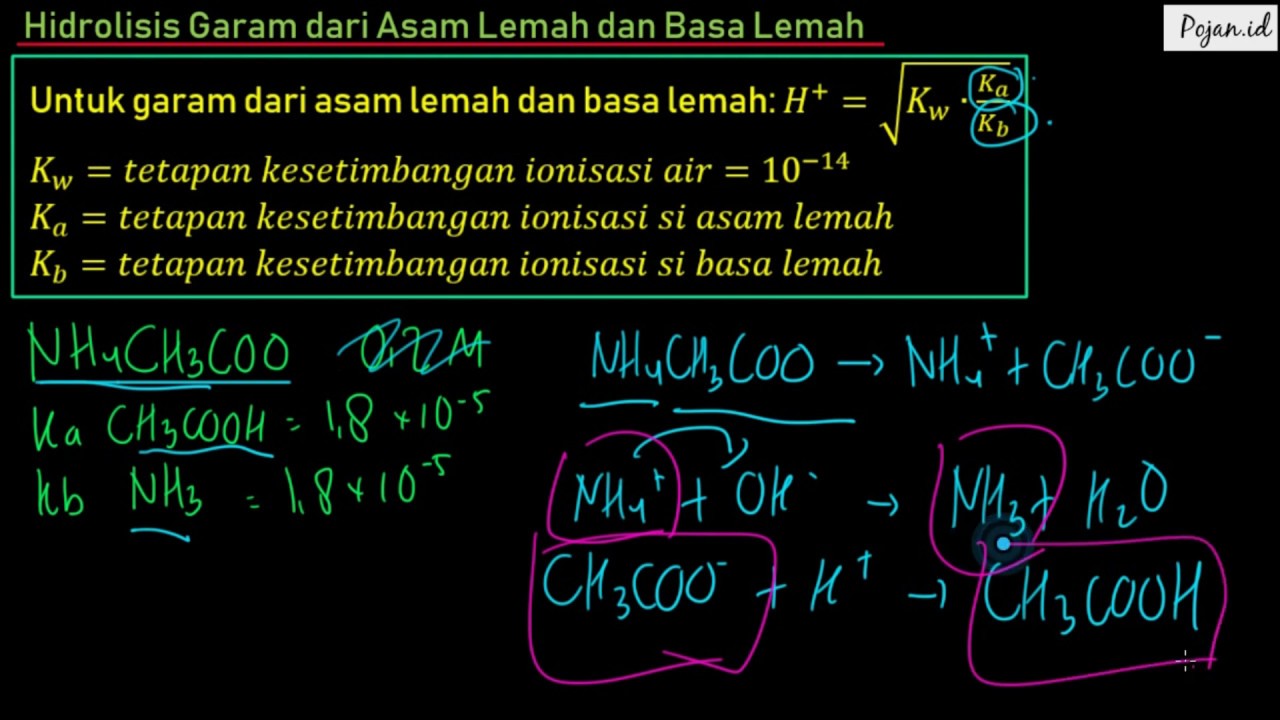
Hidrolisis Garam dari Asam Lemah dan Basa Lemah Materi Hidrolisis
Hidrolisis sendiri berasal dari kata "hydro" dan "lysis" yang jika diartikan kata per kata menjadi air dan penguraian. Jika digabungkan, hidrolisis berarti penguraian senyawa garam dalam air menjadi kation (ion positif) dan anion (ion negatif). Reaksi hidrolisis garam terbagi menjadi 2 macam.

20+ Contoh Soal Hidrolisis Asam Lemah Dan Basa Kuat Contoh Soal Terbaru
Untuk memahami konsep ini, kamu bisa pelajari di Wardaya College. Wardaya College memberikan banyak video untuk kamu yang ingin mempelajari mengenai ilmu fisika, terutama mengenai larutan buffer (penyangga). Selain itu, kamu bisa mengerjakan contoh soal larutan penyangga yang akan menguji kemampuan kamu.

Contoh Soal Hidrolisis Garam Dan Pembahasannya Foto Modis
Rumus: Keterangan: Kh: Konstanta hidrolisis. Kw: Konstanta air.

Perhatikan tabel persamaan reaksi hidrolisis garam beriku...
1. Diketahui volume larutan (NH adalah 250 mL. Jika molaritas sebesar (NH 0,1M dan Kb = 2 x 10 . Tentukan pH larutan tersebut! V = 250 mL Molaritas = 0,1 M Kb = 2 x 10 pH larutan (NH 2. Jika diketahui Ka larutan CH dan memiliki molaritas sebesar 0,1 M. Hitunglah pH larutan CH Molaritas = 0,1 M

Rumus Penyangga Dan Hidrolisis PDF
Tipe soal I: Jika diketahui di soal hanya garam maka langsung masuk rumus. Contoh Soal: Tentukan pH dari larutan CH 3 COONa 0,1 M (Ka CH 3 COOH = 10-5). Ciri Hidrolisis. Asam dan Basa akan habis. Menentukan M garam. Masuk Rumus : pOH = 4,5. pH = 14 - 4,5 = 9,5. Garam dari asam lemah dan basa lemah. (Hidrolisis sempurna)

Hidrolisis Garam
Hidrolisis garam yakni reaksi penguraian yang terjadi antara kation dan anion garam dengan air dalam suatu larutan. Catatan: hidrolisis berasal dari kata hydro artinya air dan lysis artinya penguraian. Sifat dari hidrolisis garam yakni: Garam merupakan pembentukan asam dan basa.

Rumus Hidrolisis PDF
Pengertian Hidrolisis Reaksi pada Hidrolisis Garam Cara Menghitung Nilai pH Contoh Soal 1 Contoh Soal 2 Manfaat Hidrolisis Garam dalam Kehidupan Pengertian Garam Garam merupakan senyawa yang dihasilkan dari reaksi netralisasi antara larutan asam dan larutan basa. Secara umum reaksi netralisasi adalah sebagai berikut:
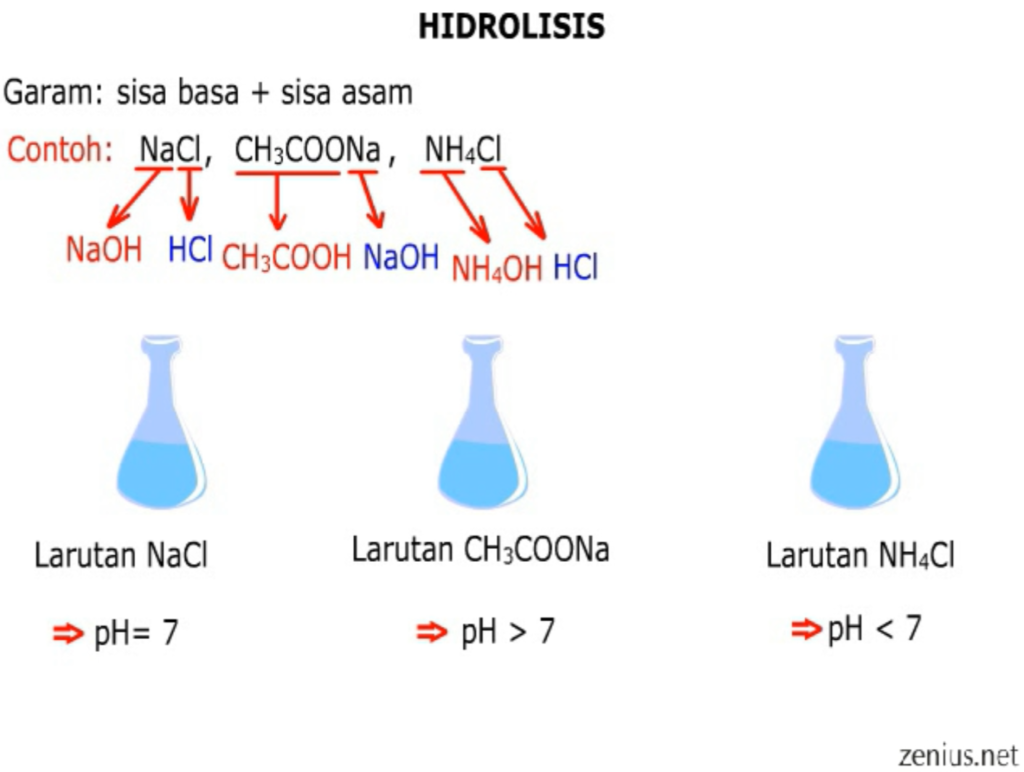
Hidrolisis Garam Materi Kimia Kelas 11
Rumus tetapan hidrolisis (Kh) adalah sebagai berikut: 1. Rumus tetapan hidrolisis garam yang berasal dari asam kuat dan basa kuat Karena perbandingan [H +] dan [OH - ] sama, maka larutan bersifat netral sehingga kita tidak memerlukan Kh untuk menghitung pH larutan tersebut, karena sudah dipastikan pH = 7. 2.

Derajat hidrolisis dari larutan NH4Cl 0,001 M adalah(...
BH + (aq) ⇌ B (aq) + H + (aq) Dengan asumsi jumlah kation BH + yang terhidrolisis relatif kecil ( [BH +] setimbang ≈ [BH +] awal = M b ), sebagaimana kation terhidrolisis merupakan asam konjugasi lemah, maka pada kondisi setimbang:
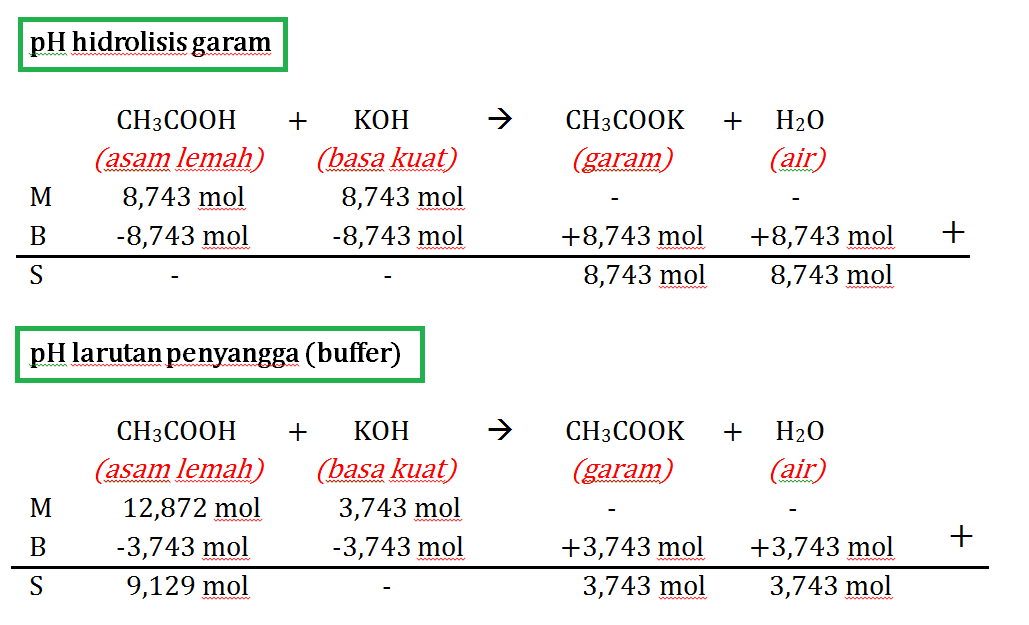
Rumus Hidrolisis mertqdate
Jenis hidrolisis garam. Hidrolisis garam dari asam lemah dan basa kuat; Jika suatu garam dari asam lemah dan basa kuat dilarutkan dalam air, maka kation dari basa kuat tidak terhidrolisis sedangkan anion dari asam lemah mengalami hidrolisis. Rumus yang berlaku pada hidrolisis garam dari asam lemah dan basa kuat sebagai berikut:

Soal Hidrolisis Garam Dan Penyelesaiannya
Hidrolisis adalah reaksi kimia antara suatu zat dengan air, yang menghasilkan perubahan sifat kimia zat tersebut. Hidrolisis dapat terjadi pada berbagai jenis zat, seperti garam, asam, basa, ester, dan amida. Supaya lebih memahami tentang rumus hidrolisis ini, berikut ulasan lengkap rumus hidrolisis mulai dari definisi, sifat, macam-macam.

RumusRumus Hidrolisis Garam PDF
Oleh karena itu garam dapat terbentuk dari 4 reaksi hidrolisis kimia sebagai berikut: Garam yang berasal dari asam lemah dan basa kuat bersifat netral dan memiliki pH = 7, yang artinya tidak terjadi hidrolisis. Garam dari asam kuat dan basa lemah, di mana garam ini akan memiliki pH < 7 alias bersifat asam. Garam dari asam lemah dan basa kuat.

LENGKAP ‼️ CARA MENGHITUNG pH HIDROLISIS GARAM KELAS 11 YouTube
Hidrolisis merupakam istilah umum untuk reaksi suatu zat dengan air. Lebih lanjut, hidrolisis adalah reaksi penguraian garam oleh air (H 2 O) atau reaksi ion-ion garam dengan air yang akan menghasilkan asam dan/atau basa. Air (H 2 O) akan diurai menjadi kation H + (hidrogen) dan anion OH - (hidroksida).

Persamaan Reaksi Hidrolisis Yang Tepat Untuk Garam Yang Bersifat Basa
Sehingga, hidrolisis garam adalah reaksi antara salah satu ion-ion garam (kation atau anion) dengan air dan membentuk larutan bersifat asam atau basa. Sifat asam atau basa larutan yang dihasilkan hidrolisis garam bergantung pada jenis asam basa yang membentuk garam tersebut. Baca juga: Hukum Kekekalan Energi: Pengertian, Rumus, dan Penerapannya